Ngừng sản xuất, sử dụng thuốc gây tê tủy sống Bupivacaine WPW nghi gây tai biến sản khoa
 Thu hồi toàn quốc thuốc Aciclovir do Công ty cổ phần Dược vật tư y tế Hải Dương sản xuất Thu hồi toàn quốc thuốc Aciclovir do Công ty cổ phần Dược vật tư y tế Hải Dương sản xuất Cục Quản lý Dược (Bộ Y tế) vừa ra công văn số 19644/QLD-CL về việc thu hồi thuốc Aciclovir không đạt tiêu chuẩn chất lượng. ... |
 Cận cảnh thuốc gây tê tủy sống nghi gây ra 3 ca tai biến sản khoa ở Đà Nẵng Cận cảnh thuốc gây tê tủy sống nghi gây ra 3 ca tai biến sản khoa ở Đà Nẵng Nhiều sở y tế, bệnh viện các tỉnh Quảng Nam, Quảng Ngãi, Long An, Bến Tre… nghi ngờ thuốc gây tê Bupivacaine WPW Spinal 0,5% ... |
 Bộ Y tế vào cuộc vụ hai sản phụ tử vong, một nguy kịch ở Bệnh viện Phụ nữ Đà Nẵng Bộ Y tế vào cuộc vụ hai sản phụ tử vong, một nguy kịch ở Bệnh viện Phụ nữ Đà Nẵng Vụ Sức khỏe Bà mẹ trẻ em (Bộ Y tế) yêu cầu các đơn vị liên quan phải kiểm tra, xác minh và làm rõ ... |
Công ty Cổ phần Dược phẩm Trung ương CPC I vừa có văn bản gửi các bệnh viện cho biết đã gửi thuốc Bupivacaine WPW Spinal Heavy 0,5% đi kiểm nghiệm tại Viện Kiểm nghiệm Thuốc Trung ương. Đồng thời công ty này cho biết đã dừng sản xuất loại thuốc này và đề nghị các bệnh viện tạm ngừng sử dụng cho đến khi hoàn tất việc kiểm nghiệm thuốc.
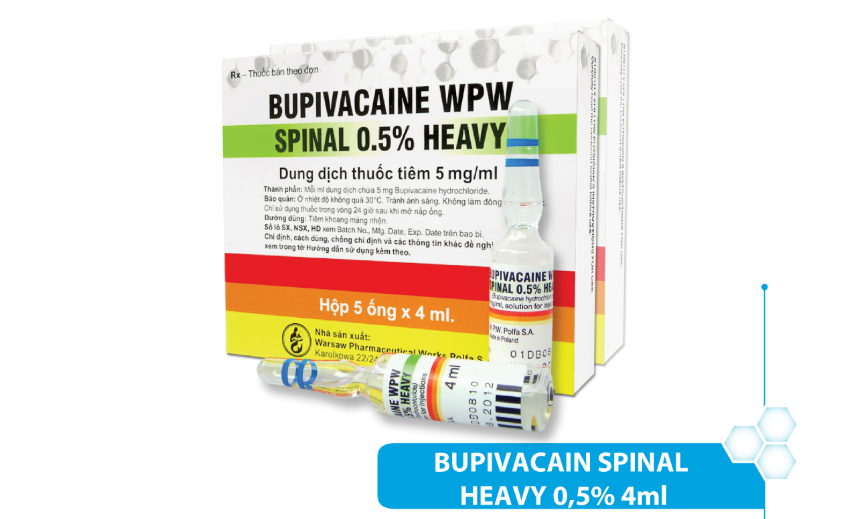 |
Thuốc tiêm gây tê tủy sống Bupivacaine WPW Spinal Heavy 0,5% đang nằm trong vòng nghi ngờ của các chuyên gia y tế, các bệnh viện, sở y tế là nguyên nhân gây ra hàng loạt tai biến sản khoa ở Đà Nẵng. Trong đó có 2 ca sản phụ tử vong, 1 ca nguy kịch sau khi dùng thuốc này.
Trước đó, ngày 22/11 Cục Quản lý Dược (Bộ Y tế) có văn bản chỉ đạo yêu cầu Công ty Cổ phần Dược phẩm Trung ương CPC I khẩn trương có giải pháp thay thế thuốc Bupivacaine WPW Spinal Heavy 0,5% trúng thầu để đảm bảo thực hiện hợp đồng ký kết theo quy định, và đảm bảo nhu cầu khám bệnh, chữa bệnh của nhân dân.
Cục Quản lý Dược cũng yêu cầu Công ty Cổ phần Dược phẩm Trung ương CPC I phải phối hợp với các đơn vị chức năng triển khai các nội dung theo chỉ đạo của Cục, đồng thời gửi báo cáo về giải pháp thay thế thuốc Bupivacaine trước ngày 26/11/2019.
Cục Quản lý Dược, hiện có 18 thuốc tiêm chứa hoạt chất tương tự sản phẩm liên quan tai biến của các nhà sản xuất từ: Pháp, Ấn Độ và Việt Nam được cấp visa lưu hành tại Việt Nam.
Cục Quản lý Dược yêu cầu các Sở Y tế tỉnh, thành phố và các bệnh viện rà soát lại danh mục thuốc trúng thầu. Ngoài 3 ca tai biến xảy ra tại Đà Nẵng còn có những trường hợp tương tự xảy ra ở những địa phương khác, như ở Cần Thơ và những nơi đang có thống kê gửi về Bộ Y tế.
Tin bài liên quan
Các tin bài khác

Lựa chọn Việt Nam mổ u não, bệnh nhân Campuchia phục hồi khả năng vận động và giao tiếp chỉ sau 6 ngày

Dấu ấn thầm lặng của bầu Hiển trong chiến tích của U17 Việt Nam

Cuộc thi nhan sắc dành cho nữ doanh nhân (Mrs Cosmos Việt Nam 2026) chính thức ra mắt

Vinmec Đà Nẵng cứu sống du khách quốc tế bị tắc mạch phổi nguy kịch trên tàu du lịch
Đọc nhiều

Peace Trees Việt Nam hỗ trợ Quảng Trị nâng cao chất lượng giáo dục

Mở rộng kết nối kinh tế, văn hóa và giao lưu nhân dân Việt Nam - Armenia

MTTQ Việt Nam và Chính hiệp toàn quốc Trung Quốc thúc đẩy hợp tác, tăng cường giao lưu nhân dân
![[Video] Lào dành ưu tiên hàng đầu cho quan hệ với Việt Nam](https://thoidai.com.vn/stores/news_dataimages/2026/062026/09/08/croped/thumbnail/thu-tu-o-ng-la-o-cover20260609081550.jpg?260609110133)
[Video] Lào dành ưu tiên hàng đầu cho quan hệ với Việt Nam
Bờ cõi biển đảo
Miền đất - Con người Cuộc sống vùng biên Nhịp sống biển đảo Lịch sử chủ quyền Giao lưu hữu nghị

Lan tỏa tình yêu biển, đảo của Tổ quốc tại tỉnh Đắk Lắk

Từ một lá thư nơi cực Tây Tổ quốc đến sự hồi sinh của điểm trường vùng biên

Tàu buồm hải quân hoàn thành chuyến đối ngoại quốc phòng tại Thái Lan và Campuchia
Multimedia

Một số mốc thời gian quan trọng sắp xếp, tổ chức lại thôn, tổ dân phố

Nhật Bản là đối tác kinh tế quan trọng hàng đầu của Việt Nam

[Infographic] 9 luật và 31 nghị quyết được thông qua tại Kỳ họp thứ nhất, Quốc hội khóa XVI

[Infographic] Việt Nam và Trung Quốc ký kết 32 văn kiện hợp tác

Chính phủ nhiệm kỳ Quốc hội khóa XVI có 14 Bộ, 3 cơ quan ngang Bộ

[Infographic] Các mốc thời gian sau cuộc bầu cử Đại biểu Quốc hội khóa XVI và đại biểu HĐND các cấp

[Infographic] Bầu cử Quốc hội và HĐND: Cách tra cứu thông tin về người ứng cử trên VNeID
Thánh đường Hồi giáo Al-noor - Không gian tôn giáo giữa lòng Hà Nội
![[Video] Đối ngoại nhân dân Thủ đô hướng tới kết nối hiệu quả nguồn lực người Việt Nam ở nước ngoài](https://thoidai.com.vn/stores/news_dataimages/2026/062026/10/16/video-doi-ngoai-nhan-dan-thu-do-huong-toi-ket-noi-hieu-qua-nguon-luc-nguoi-viet-nam-o-nuoc-ngoai-20260610161424.jpg?rt=20260610161459?260610045832)
[Video] Đối ngoại nhân dân Thủ đô hướng tới kết nối hiệu quả nguồn lực người Việt Nam ở nước ngoài
![[Video] Plan International đồng hành cùng thanh thiếu nhi tiên phong ứng phó với biến đổi khí hậu](https://thoidai.com.vn/stores/news_dataimages/2026/062026/09/14/plan-international-dong-hanh-cung-thanh-thieu-nhi-tien-phong-ung-pho-voi-bien-doi-khi-hau-20260609144229.jpg?rt=20260609144235?260609050709)
[Video] Plan International đồng hành cùng thanh thiếu nhi tiên phong ứng phó với biến đổi khí hậu
![[Video] Lào dành ưu tiên hàng đầu cho quan hệ với Việt Nam](https://thoidai.com.vn/stores/news_dataimages/2026/062026/09/08/croped/thu-tu-o-ng-la-o-cover20260609081550.jpg?260609110133)
[Video] Lào dành ưu tiên hàng đầu cho quan hệ với Việt Nam
![[Video] Doanh nghiệp Hoa Kỳ hỗ trợ Việt Nam xác định danh tính người mất tích trong chiến tranh](https://thoidai.com.vn/stores/news_dataimages/2026/062026/02/11/croped/vie-t-my-cover20260602115259.jpg?260602083849)
[Video] Doanh nghiệp Hoa Kỳ hỗ trợ Việt Nam xác định danh tính người mất tích trong chiến tranh
![[Video] Nguyên Phó Chủ tịch nước Nguyễn Thị Bình nhận Huân chương “Ngôi sao Công trạng” của Nhà nước Palestine](https://thoidai.com.vn/stores/news_dataimages/2026/052026/22/21/croped/trao-hua-n-chu-o-ng-cover20260522210759.jpg?260523104103)
[Video] Nguyên Phó Chủ tịch nước Nguyễn Thị Bình nhận Huân chương “Ngôi sao Công trạng” của Nhà nước Palestine
![[Video] GNI khánh thành thư viện KB trị giá hơn 1,9 tỷ đồng tại Tuyên Quang](https://thoidai.com.vn/stores/news_dataimages/2026/052026/22/15/video-gni-khanh-thanh-thu-vien-kb-tri-gia-hon-19-ty-dong-tai-tuyen-quang-20260522152939.jpg?rt=20260522152942?260522084551)
[Video] GNI khánh thành thư viện KB trị giá hơn 1,9 tỷ đồng tại Tuyên Quang
![[Video] Quảng Trị thúc đẩy dinh dưỡng học đường: Đầu tư cho trẻ em từ bữa ăn mỗi ngày](https://thoidai.com.vn/stores/news_dataimages/2026/052026/22/14/video-quang-tri-thuc-day-dinh-duong-hoc-duong-dau-tu-cho-tre-em-tu-bua-an-moi-ngay-20260522144849.jpg?rt=20260522144855?260522084534)
[Video] Quảng Trị thúc đẩy dinh dưỡng học đường: Đầu tư cho trẻ em từ bữa ăn mỗi ngày
![[Video] Dấu ấn của Đại sứ Nicolai Prytz trong thúc đẩy hợp tác, giao lưu nhân dân Việt Nam - Đan Mạch](https://thoidai.com.vn/stores/news_dataimages/2026/052026/21/10/croped/da-i-su-dan-ma-ch-cover20260521101628.jpg?260521045701)
[Video] Dấu ấn của Đại sứ Nicolai Prytz trong thúc đẩy hợp tác, giao lưu nhân dân Việt Nam - Đan Mạch
![[Video] Người bạn Palestine gắn bó hơn 40 năm với Việt Nam nhận Kỷ niệm chương](https://thoidai.com.vn/stores/news_dataimages/2026/052026/21/10/croped/da-i-su-plestine-cover20260521102907.jpg?260521045633)
[Video] Người bạn Palestine gắn bó hơn 40 năm với Việt Nam nhận Kỷ niệm chương
![[Video] Thánh đường Hồi giáo Al-noor - Không gian tôn giáo giữa lòng Hà Nội](https://thoidai.com.vn/stores/news_dataimages/2026/052026/22/14/video-thanh-duong-hoi-giao-al-noor-khong-gian-ton-giao-giua-long-ha-noi-20260522144501.jpg?rt=20260522144507?260522084610)
[Video] Thánh đường Hồi giáo Al-noor - Không gian tôn giáo giữa lòng Hà Nội
![[Video] Cử tri cả nước nô nức đi bầu cử đại biểu Quốc hội khóa XVI và HĐND các cấp](https://thoidai.com.vn/stores/news_dataimages/2026/032026/15/15/croped/nga-y-ba-u-cu-cover20260315150902.jpg?260316093218)
[Video] Cử tri cả nước nô nức đi bầu cử đại biểu Quốc hội khóa XVI và HĐND các cấp
![[VIDEO] Tinh thần dân chủ của nhân dân Việt Nam trong bầu cử](https://thoidai.com.vn/stores/news_dataimages/2026/032026/13/15/croped/pv-da-i-su-la-o-cover20260313153333.jpg?260316091846)
[VIDEO] Tinh thần dân chủ của nhân dân Việt Nam trong bầu cử

Tổ chức Giao lưu Quốc tế Việt Nam Nhật Bản (FAVIJA): thúc đẩy hữu nghị, hợp tác đa phương
![[Video] Vũ điệu chúc xuân sôi động của Đại sứ Hà Lan tại Việt Nam](https://thoidai.com.vn/stores/news_dataimages/2026/022026/13/06/croped/video-dai-su-ha-lan-tai-viet-nam-gui-loi-chuc-tet-bang-vu-dieu-soi-dong-20260213062706.jpg?260213053058)
[Video] Vũ điệu chúc xuân sôi động của Đại sứ Hà Lan tại Việt Nam
![[Video] Đại sứ Lào tại Việt Nam tin tưởng Đại hội XIV sẽ tạo động lực mạnh mẽ cho Việt Nam phát triển toàn diện](https://thoidai.com.vn/stores/news_dataimages/2026/012026/19/10/video-dai-su-lao-tai-viet-nam-tin-tuong-dai-hoi-xiv-se-tao-dong-luc-manh-me-cho-viet-nam-phat-trien-toan-dien-20260119100621.jpg?rt=20260119100624?260119015548)









